
相较其他传统的医学手段,干细胞产品及药品更为复杂,可以说是一种有生命的活药。若要在临床转化中取得理想的效果,从源头就要遵循严苛的制备工艺和质控标准!细胞制备生产整个过程中,发生较小的偏差都会导致临床结果大相径庭,甚至影响其安全性,对受者造成不可估量的健康危害。
随着我国《干细胞临床研究管理办法》的颁布实施,开展干细胞临床研究需取得卫健委和国家药监局的批准,临床伦理上规定开展临床研究的及药品申报的干细胞产品,需取得第三方生物制剂检验机构出具的质量检测报告。
而中国食品药品检定研究院(简称“中检院”),是目前受细胞行业颇为认可的第三方检测机构,也是具有(CMA)资格的干细胞质量复核机构。取得中检院质量认定,被认为是进行干细胞药品申报的基础条件之一。也标志该企业从细胞制剂的生产工艺到质量控制体系,均符合药品申报的前提,是具备临床级别干细胞制剂生产的能力的象征。
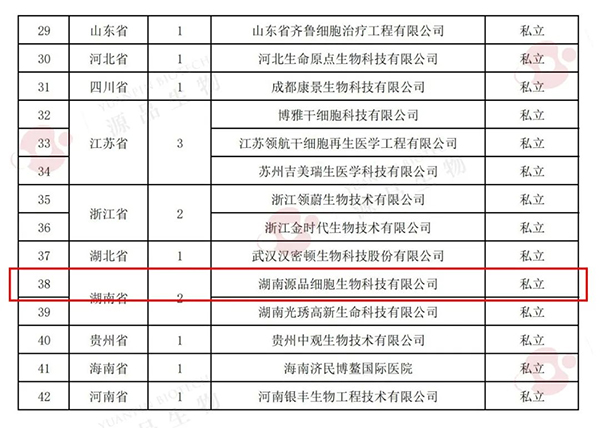
截至目前,全国共有42家机构获得中检院质量认定,源品生物是湖南省2家机构之一。

源品生物
技术至精、质量至臻
自2020年10月16日至今,源品生物已送检9个批次的脐带间充质干细胞至中国食品药品检定研究院。分别于2021年4月、7月获得6个批次脐带间充质干细胞的质量《检验报告》,涉及细胞质量四大体系全方位多项目检验,包括基本生物学属性、微生物学安全性、生物学安全性、生物学有效性共38项检测。检验结果经检验,每一份送检细胞(含3个不同代次)38项检测结果均合格。
检验报告结论证明:源品生物的脐带间充质干细胞(Mesenchymal Stem Cells,MSCs)产品在其生产工艺稳定性和细胞质量方面,达到了临床应用级别,再次证实源品生物脐带间充质干细胞其生物学属性、微生物学安全性、生物学安全性和有效性均已达到临床应用安全的最高标准。源品生物作为湖南省唯二获得中检院报告的干细胞企业,深度诠释了源品在行业内技术至精、质量至臻的专业高度和技术权威,也为公司在临床广泛开展针对不同的适应症的临床研究及后续转化提供更为坚实的基础。

▲ 源品生物获中国最专业、最权威的中国食品药品检定研究院颁发细胞质量《检验报告》
在以中国干细胞产业创始人之一王健教授为核心的具有多年细胞制备经验的“细胞工匠”们组成的生产制备团队与质量管控团队的努力下,源品生物短短半年内建立了由400余个质量管理文件、二大质量检测监督体系(QA、QC)、三大质量管理文件体系(SMP、SOP、STP)组成的质量管理体系,并取得了ISO-9001质量管理体系国际认证。
此前,源品生物先后通过中国生物医药技术协会干细胞制剂制备质量管理与细胞库质量管理两大体系的认证,成为中国第一家获中国医药生物技术协会"双认证"的干细胞企业,创造了干细胞与再生医学行业新的历史!

源品生物一直视质量为生命,确保源品生物出品的每一份细胞,拥有行业内最高标准的质量保障。我们也将长期践行严格的质控,不断优化生产工艺,将一直保持严苛的标准,树立细胞产品质量标杆。
 扫一扫咨询微信客服
扫一扫咨询微信客服